
تصویری: مدل بور چگونه طیف اتمی را توضیح می دهد؟
2024 نویسنده: Miles Stephen | [email protected]. آخرین اصلاح شده: 2023-12-15 23:35
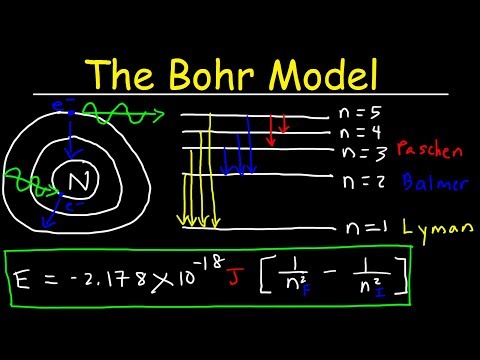
نیلز بور توضیح داد را طیف خطی از هیدروژن اتم با فرض اینکه الکترون در مدارهای دایره ای حرکت می کند و مدارهایی با شعاع های معینی مجاز هستند. نزدیکترین مدار به هسته نشان دهنده وضعیت پایه هسته است اتم و پایدارترین بود. مدارهای دورتر حالت های برانگیخته با انرژی بالاتر بودند.
به طور مشابه، مدل بور چه چیزی را توضیح می دهد؟
را مدل بور نشان میدهد که الکترونهای اتمها در مدارهایی با انرژی متفاوت به دور هسته قرار دارند (سیارهها را در نظر بگیرید که به دور خورشید میچرخند). بور از اصطلاح سطوح انرژی (یا پوسته) برای توصیف این مدارهای انرژی متفاوت استفاده کرد.
علاوه بر این، چگونه یک مدل بور را می خوانید؟
- هسته را رسم کنید.
- تعداد نوترون ها و تعداد پروتون های هسته را بنویسید.
- اولین سطح انرژی را رسم کنید.
- الکترون های موجود در سطوح انرژی را طبق قوانین زیر رسم کنید.
- تعداد الکترونهایی که در هر سطح قرار میگیرند و تعداد الکترونهای باقیمانده برای استفاده را پیگیری کنید.
به همین ترتیب ممکن است سوال شود که چگونه یک طیف اتمی تولید می شود؟
چه زمانی اتم ها آنها برانگیخته می شوند، آنها نورهایی با طول موج های مشخصی را ساطع می کنند که با رنگ های مختلف مطابقت دارد. نور ساطع شده را می توان به صورت مجموعه ای از خطوط رنگی با فضاهای تاریک در میان مشاهده کرد. به این سری از خطوط رنگی خط یا خط می گویند طیف اتمی . هر عنصر تولید می کند مجموعه ای منحصر به فرد از طیفی خطوط
بور در مدل خود چه نتیجه ای برای توضیح طیف خطی هیدروژن گرفت؟
توضیح: بور این فرض را بر این واقعیت استوار کرد که فقط تعداد کمی وجود دارد خطوط در طیف از هیدروژن اتم و او معتقد بود که خطوط در نتیجه نور آزاد شده یا جذب الکترون از مداری به مدار دیگر در اتم بود.
توصیه شده:
چگونه طیف های گسیلی شواهدی برای پوسته های الکترونی در مدل بور هستند؟

وجود تنها خطوط معین در طیف اتمی به این معنی است که یک الکترون فقط می تواند سطوح انرژی گسسته خاصی را اتخاذ کند (انرژی کوانتیزه می شود). از این رو ایده پوسته های کوانتومی است. فرکانس های فوتون جذب یا گسیل شده توسط یک اتم با تفاوت بین سطوح انرژی مدارها ثابت می شود
طیف گسیل اتمی چه تفاوتی با طیف پیوسته دارد؟

طیف پیوسته: طیفی که دارای تمام طول موج ها بدون شکاف در یک محدوده وسیع است. طیف گسیل: هنگامی که یک الکترون در حالت برانگیخته به سطح انرژی پایین تری حرکت می کند، مقدار مشخصی انرژی را به صورت فوتون ساطع می کند. طیف این انتقال از خطوط تشکیل شده است زیرا سطوح انرژی کوانتیزه شده است
چگونه بور مدل اتمی رادرفورد را بهبود بخشید؟

بور مدل اتمی رادرفورد را با پیشنهاد اینکه الکترون ها در مدارهای دایره ای با سطوح انرژی خاص حرکت می کنند، بهبود بخشید. توضیح: رادرفورد پیشنهاد کرد که الکترونها مانند سیارات به دور خورشید دور هسته میچرخند. هنگامی که یک اتم فلز گرم می شود، انرژی جذب می کند و الکترون ها به سطوح انرژی بالاتر می پرند
انواع امواج لرزه ای را توضیح می دهد که هر کدام از آنها را توضیح می دهد؟

زمین لرزه ها سه نوع امواج لرزه ای ایجاد می کنند: امواج اولیه، امواج ثانویه و امواج سطحی. هر نوع از مواد به طور متفاوتی حرکت می کند. علاوه بر این، امواج می توانند از مرزهای بین لایه های مختلف منعکس یا جهش کنند. امواج همچنین می توانند هنگام عبور از یک لایه به لایه دیگر خم شوند
نیلز بور چگونه الکترون ها را در مدل اتمی خود توصیف کرد؟
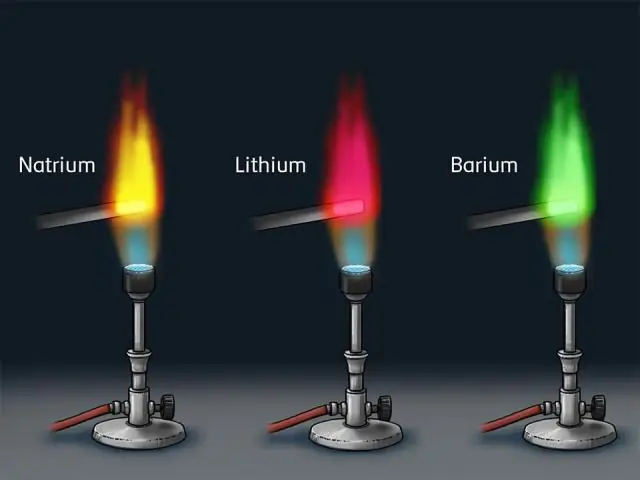
مدل اتمی بور: در سال 1913 بور مدل پوسته کوانتیزه شده خود را از اتم پیشنهاد کرد تا توضیح دهد چگونه الکترون ها می توانند مدارهای پایداری در اطراف هسته داشته باشند. انرژی یک الکترون به اندازه مدار بستگی دارد و برای مدارهای کوچکتر کمتر است. تابش تنها زمانی رخ می دهد که الکترون از یک مدار به مدار دیگر بپرد
