فهرست مطالب:

تصویری: رابطه ریاضی بین فرورفتگی نقطه انجماد و مولالیته چیست؟

2024 نویسنده: Miles Stephen | [email protected]. آخرین اصلاح شده: 2023-12-15 23:35
افسردگی نقطه انجماد یک ویژگی جمعی است که در محلول هایی که از معرفی از مولکول های املاح به یک حلال. نقطه انجماد محلول ها همگی کمتر از حلال خالص است و با مولالیته املاح رابطه مستقیم دارد.
به همین ترتیب، چگونه Molality را از فرورفتگی نقطه انجماد محاسبه می کنید؟
استراتژی:
- مرحله 1: فرورفتگی نقطه انجماد بنزن را محاسبه کنید. تیf = (نقطه انجماد حلال خالص) - (نقطه انجماد محلول)
- مرحله 2: غلظت مولی محلول را محاسبه کنید. مولالیته = مول املاح / کیلوگرم حلال.
- مرحله 3: K را محاسبه کنیدf از محلول تیf = (Kf) (متر)
به همین ترتیب، چرا از Molality در نقطه انجماد استفاده می شود؟ Wendy K. خواص کولیگاتیو خواص فیزیکی محلول ها مانند جوشیدن هستند نقطه ارتفاع و نقطه انجماد افسردگی. به همین دلیل است که استفاده می کنیم مولالیته (مول املاح در هر کیلوگرم حلال) زیرا کیلوگرم حلال با آن تغییر نمی کند درجه حرارت.
همچنین سوال این است که منظور شما از فرورفتگی نقطه انجماد چیست؟
افسردگی نقطه انجماد زمانی رخ می دهد که نقطه انجماد از یک مایع پایین می آید یا افسرده با افزودن ترکیب دیگری به آن. راه حل پایین تر است نقطه انجماد از حلال خالص.
Molality چگونه بر نقطه جوش تأثیر می گذارد؟
هر چه غلظت بالاتر باشد ( مولالیته ، هر چه بالاتر باشد نقطه جوش . می توانید به این فکر کنید اثر به عنوان املاح محلول که مولکول های حلال را در سطح، جایی که در آن از بین می برد غلیان رخ می دهد. بنابراین، به بالاتری نیاز دارد درجه حرارت برای اینکه مولکول های حلال کافی فرار کنند تا ادامه یابد غلیان در فشار اتمسفر
توصیه شده:
رابطه ریاضی بین مقاومت جریان و گیزمو ولتاژ چیست؟
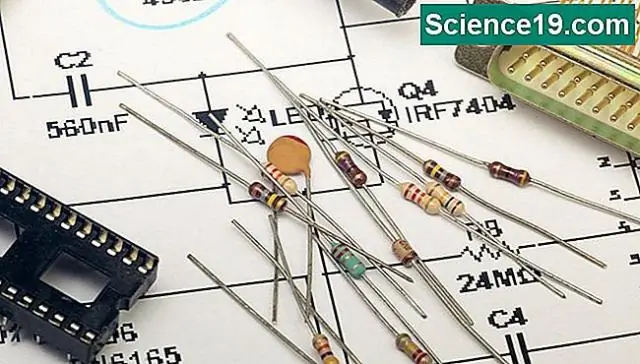
قانون اهم. رابطه بین ولتاژ، جریان و مقاومت توسط قانون اهم توضیح داده شده است. این معادله، i = v/r، به ما می گوید که جریان i که از مدار می گذرد با ولتاژ v نسبت مستقیم و با مقاومت r نسبت معکوس دارد
چگونه جرم مولی را از نقطه انجماد پیدا می کنید؟

مرحله 1: مقادیر شناخته شده را فهرست کنید و مشکل را برنامه ریزی کنید. برای محاسبه مولالیته محلول از فرورفتگی نقطه آزاد egin{align*}(Delta T_f)end{align*} استفاده کنید. سپس از معادله مولالیته برای محاسبه مول های املاح استفاده کنید. سپس گرم املاح را بر مول تقسیم کنید تا جرم مولی مشخص شود
چگونه نقطه انجماد را تعیین می کنید؟
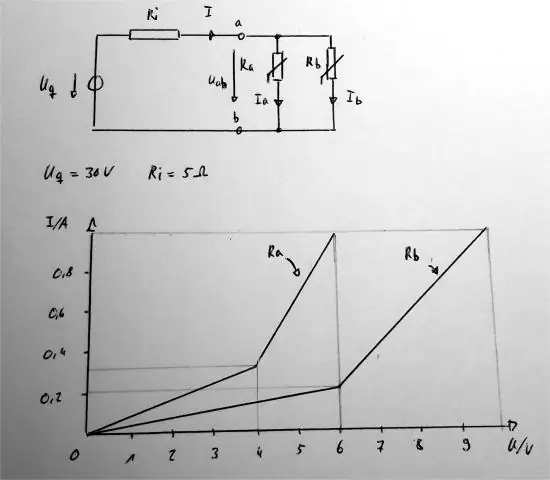
استراتژی: مرحله 1: فرورفتگی نقطه انجماد بنزن را محاسبه کنید. Tf = (نقطه انجماد حلال خالص) - (نقطه انجماد محلول) مرحله 2: غلظت مولی محلول را محاسبه کنید. مولالیته = مول املاح / کیلوگرم حلال. مرحله 3: Kf محلول را محاسبه کنید. Tf = (Kf) (m)
فرورفتگی نقطه انجماد چگونه بر وزن مولکولی تأثیر می گذارد؟

بنابراین، با افزایش جرم مولی، فرورفتگی نقطه انجماد کاهش می یابد. یعنی افزایش جرم مولی (یا مولکولی) تاثیر کمتری بر نقطه انجماد خواهد داشت
نقطه جوش و انجماد ذوب چیست؟

وقتی یک جامد به مایع تبدیل می شود به آن ذوب می گویند. نقطه ذوب آب 0 درجه سانتیگراد (32 درجه فارنهایت) است. وقتی برعکس اتفاق می افتد و مایعی به جامد تبدیل می شود به آن انجماد می گویند. جوشاندن و تراکم. هنگامی که یک مایع به گاز تبدیل می شود به آن جوش یا تبخیر می گویند
